Mais um daqueles badulaques que podem agradar os químicos.
Bijuterias para químicos não são novidade, mas a inovação deste artesanato é usar a tabela periódica como inspiração.

Mais um daqueles badulaques que podem agradar os químicos.
Bijuterias para químicos não são novidade, mas a inovação deste artesanato é usar a tabela periódica como inspiração.


O cério (Ce) é utilizado na composição de fornos auto-limpantes, para obter vidros de cor amarela e é também empregado em síntese orgênica.
Veja estas e outras informações no vídeo abaixo.
O vídeo tem legendas em português!
Uma interessante camiseta apresenta uma relação da porcentagem mássica dos elementos químicos presentes no corpo humano.
Analisando os números é possível perceber que para uma pessoa que pesa 70kg, o corpo teria uma massa de 43kg de oxigênio, 16kg de carbono, 7kg de hidrogênio, 1,8kg de nitrogênio, …

Veja mais algumas informações na Wikipedia
https://en.wikipedia.org/wiki/Chemical_makeup_of_the_human_body
https://en.wikipedia.org/wiki/Composition_of_the_human_body
Fonte Geekologie
As tabelas periódicas feitas em flash tem uma boa interatividade. São de uso rápido e bem intuitivas.
Nesta tabela é possível acessar as propriedades dos elementos da tabela, incluindo informações sobre ponto de fusão, ebulição, eletronegatividade, afinidade, etc.
Confira também as valiosas informações sobre orbitais e isótopos.
No menu, no topo esquerdo da tela, você também pode escolher se quer ver informações da Wikipédia, WebElements, vídeos ou fotos ao clicar sobre cada elemento!
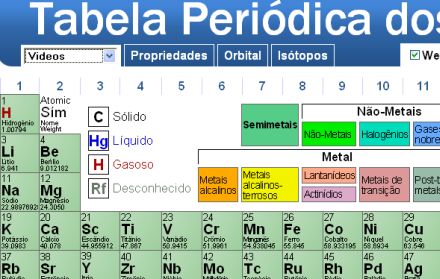
Clique para acessar
Uma versão em português está disponível em
http://www.ptable.com/
Veja também
Tabela periódica com centenas de vídeos.