Máquinas térmicas – Em elástico e calor


Vejamos o seguinte vídeo:
As máquinas térmicas são aquelas que recebem energia em forma de calor, melhor dizendo, que operam em ocasiões em que existe uma diferença de temperatura (existindo uma fonte quente e uma fonte fria). Estas máquinas não podem contrariar as leis da termodinâmica, alias… nada pode, que diz que não podemos tranformar toda a energia(calor) em trabalho, logo parte deste calor é transferido para uma fonte de menor temperatura.
No vídeo, a fonte quente é representada pela lâmpada, que cede parte do calor que gera para as borrachas. Isso faz com que as borrachas se comprimam, deslocando o centro de massa para o lado contrário à lâmpada. O restante da energia(calor) flui da fonte quente para uma fonte fria(ar), gerando trabalho.
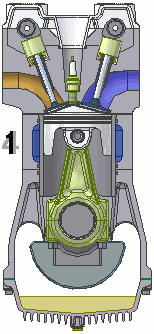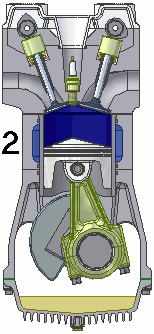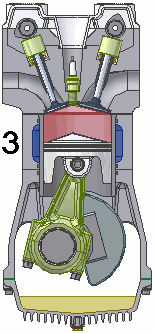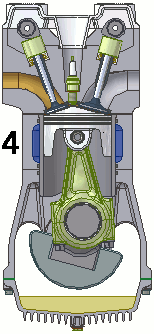
Além da máquina apresentada no video, podemos citar como exemplo carros movidos a vapor, nos quais temos uma caldeira que gera calor, parte desse calor é conduzido até um pistão que faz com que o carro se movimente, e o restante do calor e direcionado espontâneamente para uma fonte fria.
Para calcular o trabalho realizado por uma máquina térmica usamos a diferença de calor entre as fontes, como na equação seguinte:
W=Q1-Q2
Estas máquinas oferecem um rendimento, que é definido como sendo a razão entre o trabalho que a máquina fornece, W, e a energia sob a forma de calor proveniente da fonte quente, Qq, e sem o qual ela não poderia funcionar. No vídeo, a máquina apresentada possui um baixo rendimento, devido a grande perda de energia para o meio (e uma baixa diferença de temperatura entre as fontes).
Sempre se procura alcançar um rendimento máximo para essas máquinas, porém uma máquina com 100% de rendimento jamais será criada, pois essa violaria a 2ª lei da termodinâmica.
Este texto foi escrito por Cleber Klasener, como parte de um trabalho da disciplina de Físico-química I.